原料藥事業部
品質管理系統(Quality Management System, QMS)是藥品生產的核心,本公司原料藥事業部依循多項國際規範建置品質管理系統,包括GMP (Good Manufacturing Practice,優良製造規範)、GDP (Good Distribution Practice,優良運銷規範)、HACCP (Hazard Analysis and Critical Control Points,危害分析與關鍵控制點),與ICH Q10(藥品品質系統),包含推動品質風險管理(QRM)與矯正及預防措施(CAPA)機制,結合制度化管理與數據化追蹤,持續強化產品品質與安全性,並透過製程驗證、清潔規範、環境控制及供應鏈稽核,確保產品全流程的品質穩定,符合美國 FDA、歐盟 EMA、日本 PMDA 等國際監管標準。
王子製藥已建置產品實驗室,具備完整檢測能力,並依 ICH Q1A 執行長期與加速安定性試驗,確保保存期間品質穩定。關鍵檢測儀器皆依 ISO 17025(測試與校準實驗室能力標準)定期校驗,確保數據精確性。
本公司從供應商管理、生產監控、成品檢測,到市場監測,嚴格遵循品質管理流程,確認產品符合藥典標準,確保品質穩定性與合規性,更保障藥品安全與客戶信賴,展現公司對品質與永續經營的承諾。
我們採用 PDCA (Plan-Do-Check-Act)循環,及品質管理審查會議,由全廠單位共同參與,並透過建立品質管理系統中的矯正/預防措施和定期審查追蹤方式,並確保品質管理系統的適宜性、有效性和持續性,每年檢討品質改善成果。透過數據與案例檢討,設定多項持續改善行動計畫,藉此確保品質績效具體展現,並提升客戶與監管機構信賴度。
- 優化QMS(品質管理系統),降低異常批次率,提高API品質穩定性。
- 強化偏差調查機制(Deviation Investigation),確保所有異常事件均有CAPA(矯正與預防措施) 。
- 增加內部稽核(Internal Audit)頻率,從原本每年1次增加至每年2次,確保GMP符合度。
- 對API關鍵製程參數(CPP, Critical Process Parameters)進行統計分析,確保最佳製造條件。
- 增加API安定性試驗(Stability Studies)數據,確保API於不同環境條件(溫度、濕度)下仍保持有效性。
- 加強供應商的GMP稽核,確保API原料品質穩定性,降低來料變異風險。
- 提高供應商審核標準,要求供應商須符合國際標準規範,確保API原料品質。
- 建立API原料批次可追溯系統,透過條碼或區塊鏈技術確保供應鏈透明度。
- 每年定期執行GMP訓練課程,維持與提升員工品質意識;每月定期執行各單位SOP課程教育訓練,維持員工GMP精神。
保健品事業部
GMP所指的是「良好作業規範 (Good Manufacturing Practices),是一種品質管理體系,注重食品製造過程中產品的品質和安全衛生自主管理。這是一套確保產品在生產過程中符合質量標準的規範,包括原材料的選擇、設備的維護、以及生產環境的控制。GMP強調每一個生產環節的標準化,確保產品的一致性和可追溯性。另食藥署於2020年5月20日公告訂定「保健營養食品優良製造作業指引」(以下簡稱保健營養食品GMP),涵蓋製造過程中之相關作業規範,推動業者自願性驗證,精進生產製程之管理。
保健品事業部自相關規範公告訂定起,皆已完成二級品管及保健營養食品GMP,從原物料、製程中半成品、最終成品及全廠區之環境衛生等,皆遵循食品安全衛生管理法(以下簡稱食安法)及相關規範制定程序及作業標準,並確實落實自主管理,確保產品安全且品質穩定。
保健品事業部新埔廠及新埔二廠皆完成驗證符合ISO22000及HACCP品質規範,針對產品劑型及包裝型態區分9大製程,且每年重新檢視危害分析內容及重要管制點的適切性,並配合相關規範建立食品安全監測計畫,依規劃執行原料監測,確保最終產品安全性。
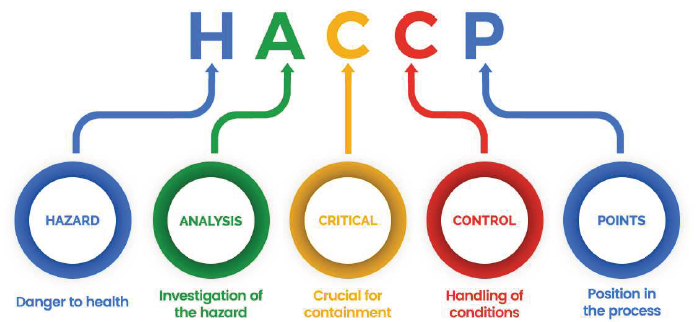
- 危害分析重要管制點系統制度 (Hazard Analysis and Critical Control Point, HACCP),HACCP 可以拆解為兩個主要的部份:HA (危害分析) 與 CCP (重要管制點) 。
- 危害分析重要管制點系統制度(HACCP)。
- HACCP是一種預防性的食品安全管理系統,通過識別和控制生產過程中的潛在危害來保障食品安全。HACCP要求企業在產品設計和生產過程中進行風險評估,並設置關鍵控制點以監控和管理這些風險。
- HA(危害分析)針對原料採收處理、食品生產過程乃至最後產品流通,以科學化及系統化分析評估各種危害發生的可能性。
- CCP(重要管制點)則是經過危害分析後,將危害發生可能性高的某一點、步驟或者程序訂為CCP,並訂定有效控制措施與條件加以預防、去除或降低食品危害至最低可以接受之程度。
- 品保/實驗室能力及認證
取得國際認證(例如:ISO22000、HACCP等)是展示企業對品質承諾的重要指標,相關品質認證不僅能夠提升市場競爭力,也為消費者提供安心的選擇。新埔廠及新埔二廠目前已取得ISO22000、HACCP、二級品管、保健營養食品GMP及清真品保系統等國際認證,包含散狀(Powder)、錠狀(Tablet)、糖衣錠狀(Sugar-coated Tablet)、膜衣錠狀(Film-coated Tablet)、膠囊狀(Capsule)等劑型種類。
廠內所使用原物料皆須依食品安全相關規範進行查核驗收,生產單位人員再依加工製程標準進行產製作業,並由IPQC人員監控並查核關鍵製程及管制項目,且成品需逐批檢驗食品衛生管制項目,並抽取成品留樣保存至該批效期,以確認產品穩定性及必要時追蹤追溯之需求。
參與能力試驗的意義,是透過公正第三方機構量化人員技術及測試品質。可依據能力試驗評比,強化實驗室內部品質保證及管制,也能經由判別實驗室偏差原因,精進實驗室技術能力,並提出有利於增加顧客信心之證明。
本公司具備先進的檢測設備和技術,並遵循公告方法建構檢驗操作標準書,能夠進行有效的產品分析與測試,確保所有產品均符合食品安全與衛生標準。此外,內部人員定期參加第三方開設的檢驗能力試驗計畫,完成評定並取得合格證書,以確認例行性檢驗作業之可信度。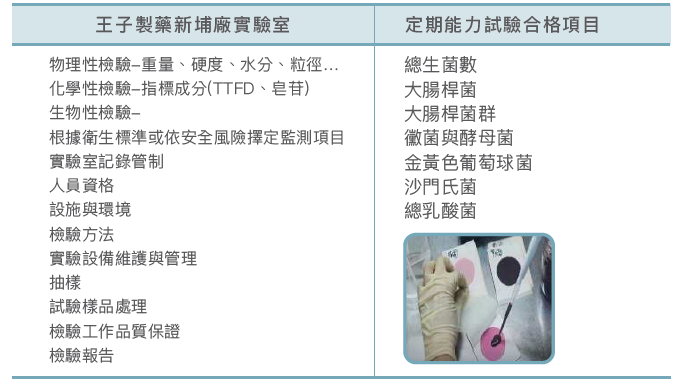
- 持續改善方案與績效
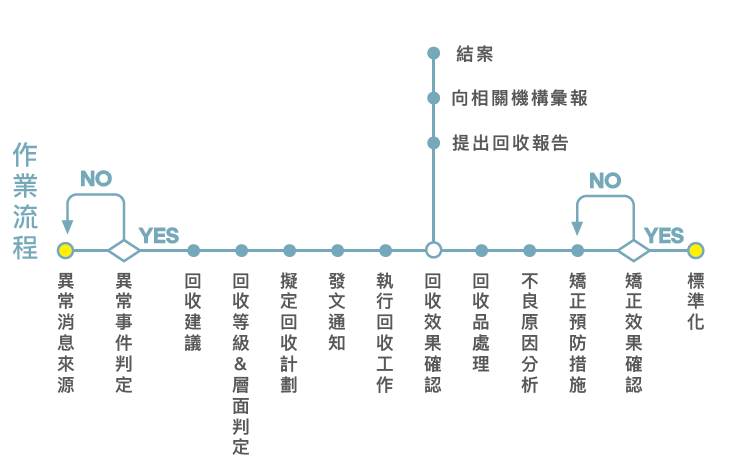
本公司品質系統具備《內部品質稽核管理程序》、《客訴處理辦法》、《不合格品管制程序》及《產品品質檢討管理辦法》等標準程序,且依規範制定《成品回收管理辦法》並定期執行模擬回收作業,當客訴異常事件發生時,皆會立即辨別影響程度並安排因應措施,必要時須立即啟動回收程序,再經異常原因分析後提出矯正預防措施,而品質單位將進行矯正措施的效果確認。
保健品事業部於2023-2024年無發生影響人體健康之異常事件,並於證書到期後接續完成二級品管及保健營養食品GMP重新驗證合格。
食品安全監測計畫及最終成品監測項目也依相關規範及食安事件等需求及考量,持續調整關注項目,以符合法規管制及衛生安全目標。